多款热门药物上市后出师不利。
经过多年艰苦的药物研发,在获得监管部门的批准后,药企得以期待着“重磅炸弹”持续的营收,让多年来的研发投资收回成本,但这一切的前提是成功的上市。
事实上,根据L.E.K.咨询报告,在2004年至2016年间批准的药物中,约有40%的药物在上市前三年的表现比销售预测低20%以上。分析显示,大多数表现不佳的公司在之后两年内也并无起色,并可能出现持续下滑的趋势。
这其中的原因各异,如生产不力、新的安全标志物、竞争对手的进入、无效营销、管理混乱,或者只是时机不当。即使这些药物当前状况稳定,但依旧会引发对其长线价值的质疑。
近日,FiercePharma总结了,近5年本应成为“重磅炸弹”上市后却低于市场预期的药物名单。
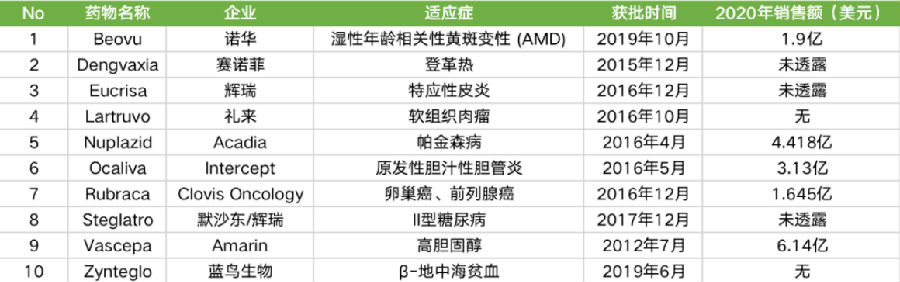
1. Beovu(诺华)
2019年10月,Beovu出现时,对再生元的Eylea和罗氏的Lucentis都构成了威胁。
Beovu可用于治疗AMD患者的时间更长,每季度或每隔一个月。在两项临床试验中,Beovu在疗效上与Eylea相匹配,甚至在减少视网膜液和中央亚视野厚度方面击败了抗VEGF药物,这是一种衡量可导致视力丧失的异常液体积聚和水肿的指标。
由此,华尔街分析师预计诺华的新眼药将在2026年位居市场榜首,并预估到2021年底,其收入约为43.8亿美元。
然而,2020年2月,美国视网膜专家协会 (ASRS) 发出警告,声称用于视网膜血管炎或眼部炎症的病例中有11例严重到足以增加视力丧失的风险。
因其安全性风险,今年截至目前,Beovu的销售额仅为8700万美元,与去年同期相比下降了16%。
2. Dengvaxia(赛诺菲)
2015年底,赛诺菲获得登革热注射剂Dengvaxia的批准时,全球医药行业似乎已准备好迎接下一次大型疫苗的“换洗”。然而两年之内,一切都变了。
菲律宾是第一个将其纳入到大型国家疫苗接种计划的国家,也是疫苗出错的地方。
上市一年后,赛诺菲披露了新的安全数据,表明对于那些之前没有感染登革热的人,使用该疫苗可能会导致更严重的情况。消息一经曝光,菲律宾立即取消了疫苗接种计划,并要求公司退款,起诉官员等。
赛诺菲花了20年时间和15亿欧元开发疫苗,多次表示该产品将成为“重磅炸弹”。但去年,赛诺菲没有披露Dengvaxia的销售额,这意味着它们对公司并不重要。
3. Eucrisa(辉瑞)
辉瑞在2016年斥资52亿美元收购Anacor,交易的核心便是crisaborole(Eucrisa),辉瑞称其峰值销售额有可能达到或超过 20 亿美元。数月后,Eucrisa被批准用于治疗特应性皮炎。
但辉瑞显然没有准备好应对赛诺菲和再生元的Dupixent的市场竞争。虽然仅比Eucrisa晚上市三个月,Dupixent依旧凭借出色的疗效数据被批准用于年仅12岁及以上的青少年患者,用于中度至重度疾病,成为该领域的首选。
即使辉瑞不断加大营销费用,但未能改变下降的局面。之后除了Dupixent这一强劲对手,更是出现了Opzelura、ARQ-151,市场竞争愈加激烈。2019年,Eucrisa的销售额为1.38亿美元,2020年的销售额也未被披露。
4. Lartruvo(礼来)
Lartruvo (olaratumab) 靶向PDGFR-α被开发用于治疗软组织肉瘤,该药物在整个监管过程中都获得了FDA的“VIP待遇”——从快速通道和突破性疗法指定到优先审查,最终在2016年10月批准。
FDA强调它是第一个新疗法软组织肉瘤 (STS) 的一线疗法。据媒体报道,华尔街分析师预测Lartruvo的销售额将在五年内达到3.7375亿美元,但这一切在2019年戛然而止。
礼来报告称,Lartruvo在第三阶段验证性试验中失败了。在整个STS人群或平滑肌肉瘤亚组中,该试验无法显示Lartruvo和多柔比星比单独使用多柔比星有延长寿命的益处。
2019年9月,礼来正式向FDA申请撤回Lartruvo。因上述撤销缘故,该公司对2019年第一季度进行了8460万美元的减值。
5. Nuplazid(Acadia)
Nuplazid首次获批用于预防帕金森病患者的幻觉和妄想后,Evaluate Pharma曾预计Nuplazid 2020年的潜在销售额为8.41亿美元。
然而,自从FDA批准以来,Nuplazid一直被安全问题、联邦营销调查和适应症扩展所拖累。2020年,Nuplazid营收仅为4.418亿美元。
与此同时,在新冠期间,医生就诊次数减少、长期护理机构的新患者人数减少都造成了Nuplazid的销售额受到打击。
6. Ocaliva(Intercept)
早在2017年,FDA就批准Ocaliva治疗罕见的肝病原发性胆汁性胆管炎,但Intercept尚未说服监管机构在非酒精性脂肪性肝炎 (NASH) 市场批准该药物。
NASH是一种主要由肥胖引起的进行性脂肪肝疾病,是很多药企的重要目标。曾有分析认为,该领域的价值可能高达数百亿,而Intercept正是曾经的领跑者。
去年夏天,FDA多次推迟对NASH药物的审查后,并表示该药物的“预期益处……仍然不确定”,并且具有一定的安全风险,这也导致了该药物去年在全球仅产生了3.13亿美元的收入。
7. Rubraca(Clovis Oncology)
Rubraca是第二个进入PARP抑制剂市场的产品,比阿斯利康和默克的 Lynparza晚了两年。但在Rubraca推出后,PARP市场发展迅速,Rubraca曾经拥有的任何优势很快就被竞争对手抹去了。
在2016年底,FDA曾授予Rubraca优先审评和突破性药物治疗的资格认定,甚至还获得过孤儿药的认定,但Rubraca却从未被认为是同类产品中最好的。
Cortellis Consensus Forecast曾预测,Rubraca在2021年的销售额可能达到6.63亿美元,但事实上,2021年上半年Rubraca的销售额仅为7490万美元。
8. Steglatro(默沙东/辉瑞)
随着糖尿病市场的迅速扩张,分析师吹捧Steglatro及其联合治疗的重磅潜力,比如与Januvia配对,或与Segluromet配合。科睿唯安和《投资者商业日报》曾预计,2022年的销售额将达到10.9亿美元。
但是,Steglatro并没有取得成功,而且很可能永远不会。
实际上,Steglatro一直处于劣势,因为它是在强生的Invokana、阿斯利康的Farxiga以及BI和礼来的Jardiance之后才进入市场的,这些药物已经达到了重磅炸弹的地位,并在2020年共带来了61.5亿美元的总销售额。
在如此市场格局中,Steglatro并未透露2020年业绩。
9. Vascepa(Amarin)
2019年,Vascepa成为首个获批用于降低甘油三酯水平升高且对他汀类药物无反应的人的心血管药物。
在看似变革性的批准之后不久,Amarin的命运发生了转变。Vascepa的数据组合以及其几项专利的无效给公司带来了可能永远无法挽回的打击。2020年3月,内华达州的宣布保护Vascepa的关键专利无效——这对Amarin来说是一个重大打击,因为它是Amarin的唯一产品。
Leerink分析师估计,到2023年,Vascepa的销售额可能会下降6%至22%,这取决于Amarin的新战略以及美国的仿制药竞争程度。
10. Zynteglo(蓝鸟生物)
Zynteglo,也称为LentiGlobin或beti-cel,是一款帮助患者产生正常水平的血红蛋白的基因疗法。
鉴于β-地中海贫血和镰状细胞病的市场潜力,Evaluate Pharma将Zynteglo列为年度最有价值的药物发布之一,估计2024年的销售额为18.7亿美元。
但在多重因素的打击下,如制造问题、新冠和安全问题,Zynteglo并未发挥出色。同时,高昂的定价(157.5万欧元)也让Zynteglo难以在欧洲市场中获利。
参考文章:
[1] Fierce Pharma:The top 10 drug launches since 2017
[2] Fierce Pharma:Failure to launch? Half of drugs rolled out since 2004 didn't live up to sales forecasts: report
[3] Fierce Pharma:Top 10 drug launch disasters
来源:思齐俱乐部









